В настоящее время для разделения мембран чаще всего применяют центрифугирование. Мембранные частицы можно разделить по скорости их седиментации или по плавучей плотности. Первый метод называется зональным центрифугированием, и разделение происходит в соответствии со значениями S, а второй - изопикническим центрифугированием, и разделение происходит в условиях равновесной плотности. На практике обычно применяют некий гибрид этих двух методов. На рис.1.7 показано положение некоторых субклеточных единиц на координантной плоскости "S-g". Садовый центр челябинск адреса топ 50 садовые центры и магазины в челябинске.
По оси абсцисс отложены коэффициенты седиментации частиц, а по оси ординат - плотность.
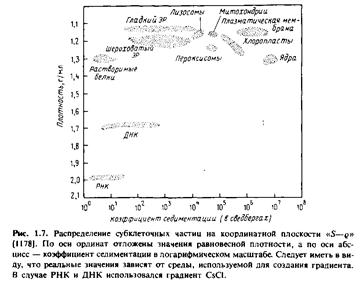
Принцип разделения по скорости седиментации можно легко уяснить, сравнив значения S для разных фракций. Например, ядра имеют относительно высокие значения S, т.е. скорость их седиментации значительно выше, чем у большинства других субклеточных органелл. Ядра можно избирательно осадить центрифугированием клеточного гомогената, при этом все другие органеллы останутся в надосадочной жидкости. В то же время гладкий и шероховатый эндоплазматический ретикулум не удается разделить с помощью зонального центрифугирования.
Для выделения различных мембранных фракций из клеточного гомогената часто используют различия в их плотности. С этой целью проводят центрифугирование в градиенте плотности. Чаще всего для создания градиента плотности используют сахарозу, однако этот метод имеет серьезные недостатки. Чтобы получить плотность, требуемую для разделения различных мембранных фракций, необходимо готовить растворы с высокой концентрацией сахарозы, которые обладают высокой вязкостью и к тому же являются гипертоничными. Внесение субклеточных органелл в гипертоничный раствор сахарозы приводит к их дегидратации, а последующее доведение раствора до изотонических условий часто сопровождается лизисом и повреждением органелл. Другая проблема состоит в том, что многие мембранные органеллы проницаемы для сахарозы. Это также может привести к осмотическому разрушению органелл. Проникновение сахарозы в разделяемые мембранные органеллы может изменить их эффективную плотность.
Таблица 1.1. Физические время все чаще используют другие среды для создания градиента плотности. Некоторые из этих сред перечислены в табл.1.1
|
Концентрация, |
Плотность, |
Вязкость, |
Осмоляльность, | |
|
% (в/о) |
г/мл |
сП |
мОсм/кг НгО | |
|
Сахароза |
20 |
1,06 |
30 |
700 |
|
Метризамид |
30 |
1,16 |
2 |
260 |
Чтобы решить эти проблемы, в последнее свойства градиентных сред.
1. Фиколл. Высокомолекулярный гидрофильный полимер сахарозы, который можно использовать для получения растворов С'Плотностью вплоть до 1,2 г/мл. Основное его преимущество состоит в низком осмотическом давлении растворов по сравнению с растворами с эквивалентной концентрацией сахарозы. Благодаря этому можно создавать растворы, изотоничные во всем диапазоне концентраций благодаря дополнительному включению в среду сахарозы или приемлемых с физиологической точки зрения солей. Недостатками являются высокая вязкость получаемых растворов и существенно нелинейная зависимость вязкости и осмолярности от концентрации.
2. Метризамид. Трииодзамещенный бензамид глюкозы Растворы метризамида имеют большую плотность, чем расторы фиколла при тех же концентрациях. Основным преимуществом растворов метризамида является их очень низкая вязкость, что позволяет ускорить разделение.35% -ный раствор метризамида имеет почти физиологическую осмолярность, так что большую часть операций в ходе разделения мембран можно проводить, не подвергая их действию гипертоничных растворов. Метризоат натрия - родственное метризамиду соединение с близкими свойствами, с тем лишь отличием, что его раствор является изотоничным при концентрации около 20%. Метризоат натрия ис- пользуют прежде всего для выделения интактных клеток. Найкоденз также является производным трииодбензойной кислоты, но имеет три гидрофильные боковые цепи. При центрифугировании он быстро образует свой собственный градиент плотности; используется для выделения субклеточных органелл.
Перколл. Коллоидная суспензия силикагеля, частички которого покрыты поливинилпирролидоном. Это покрытие ослабляет токсическое влияние силикагеля. Основным преимуществом перколла является то, что он не проникает через биологические мембраны, а его растворы имеют низкую вязкость и низкую осмолярность. Вследствие большого размера частиц центрифугирование раствора перколла при умеренных скоростях приводит к формированию градиента плотности. Поэтому разделение обычно происходит очень быстро. Среда, используемая для центрифугирования, может быть изотоничной по всему объему благодаря включению в нее солей или сахарозы. Не составляет труда создать пологий градиент, что позволяет проводить весьма эффективное разделение мембранных фракций по их плавучей плотности.
Статьи и публикации:
Объект, методы и место
исследований переработки грибов. Характеристика объекта
исследования
Целью проведенных исследований было сравнение органолептических и физико-химических показателей качества грибной продукции представленной на рынках города. Объектами исследования служили сушенные грибы теневой и тепловой видов сушки и кон ...
Разделение мембран
В настоящее время для разделения мембран чаще всего применяют центрифугирование. Мембранные частицы можно разделить по скорости их седиментации или по плавучей плотности. Первый метод называется зональным центрифугированием, и разделение ...
Исследования в области структурной и функциональной организации животных
XVIII в. ознаменовался дальнейшим углублением представлений о структурной и функциональной организации животных.
Немецкий ученый Хр. Рейль (1759–1813) основал журнал «Архив физиологии (1755) с задачей публикации результатов исследований ...

