
Девятая реакция катализируется ферментом енолазой, при этом 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту, а фосфатная связь в положении 2 становится высокоэргической. Енолаза активируется катионами Mg2+ и Mn2+ и ингибируется фторидом.

Десятая реакция характеризуется разрывом выскоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ. Катализируется ферментом пируваткиназой:

Для дествия пируваткиназы необходимы Mg2+ , а также одновалентные катионы щелочных металлов.
В результате одиннадцатой реакции пируват под влиянием пируваткарбоксилазы и при участии СО2 и АТФ карбоксилируется с образованием оксалоацетата:

Двенадцатая реакция катализируется ферментом цитрат-синтетазой, при этом ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота:

Ацетил-КоА Оксалоацетат Цитрат
Тринадцатая реакция – дегидратация лимонной кислоты с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту. Катализирует эти обратимые реакции гидратации-дегидратации фермент аконитатгидратаза. В результате происходит взаимоперемещение Н и ОН в молекуле цитрата:
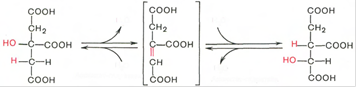
В результате четырнадцатой реакции происходит образование α-кетоглутарата. Изоцитрат дегидрируется в присутствии НАД-зависимой изоцитратдегидрогеназы. В ходе реакции изоцитрат одновременно декарбоксилируется. НАД-зависимый фермент является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ. Кроме того, фермент для проявления своей активности нуждается в ионах Mg2+ и Mn2+. Происходит выделение CO2.

В ходе пятнадцатой реакции – ферментативного восстановительного аминирования α-кетоглутаровой кислоты НАДФ-зависимой глутаматдегидрогеназой – образуется глутаминовая кислота:
НООС – СН2 – СН2 – СО – СООН + НАД(Ф)Н2 + NН3 →
НООС – СН2 – СН2 – NН2СН – СООН + НАД(Ф).
В ходе рассмотренных реакций видно, что для нормального протекания синтеза глутамата необходимо наличие в субстрате неорганического фосфорного питания, а также макро- и микроэлементов К, Mg, Mn, активирующих ферменты.
Сверхсинтез кислоты у дикого штамма возможен в специальных физиологических условиях при торможении скорости роста и увеличении проницаемости клеточной мембраны для глутаминовой кислоты. Такие условия обеспечивает определенная концентрация биотина в среде (1 – 5 мкг/л), а также присутствие некоторых антибиотиков. Внутриклеточная концентрация глутамата снижается в результате экскреции продукта в околоклеточную среду, поэтому регуляция синтеза конечным продуктом ослабевает.
Также для осуществления процесса биосинтеза глутаминовой кислоты с высоким выходом используют мутанты с нарушенной ферментативной системой превращения кетоглутаровой кислоты в янтарную (отсутствие или дефект кетоглутаратдегидрогеназы).
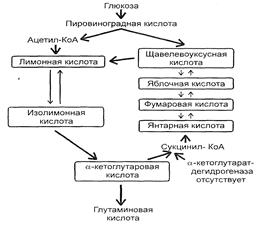
Рис. 3: Схема синтеза глутаминовой кислоты C. Glutamaticum.
Статьи и публикации:
Полиплоидия и отдалённая гибридизация в селекции растений
Виды, у которых число хромосом умножено кратно основному числу (n), называются полиплоидами
. Многие виды растений, введенные в культуру, – полиплоиды. Среди покрытосеменных растений доля полиплоидов составляет 30–35%, причём у злаковых т ...
Доказательства происхождения человека от животных
Общие черты строения человека и животных. Сравнение скелетов человека и других позвоночных, особенно млекопитающих, убедительно показывает общие черты в их строении: скелет головы, скелет туловища, скелет конечностей. В скелете конечносте ...
Регуляция секреции желудка: а) иннервация желудка, б) первая фаза
желудочной секреции (сложнорефлекторная), в) вторая и третья фазы желудочной
секреции (нейрогуморальная)
Секреция желудочных желез наступает под влиянием нервных и гуморальных раздражителей, возникающих при поступлении пищи в ЖКТ, а также при виде и запахе пищи.
Иннервация желудка. Эфферентные нервы желудок получает от парасимпатического и ...

